Загальні відомості.
Карбонат натрію технічний
(натрій вуглекислий) – порошок або гранули білого кольору. Сода кальцинована, в безводному стані представляє собою безбарвний кристалічний порошок, випускається за допомогою аміачно – содового процесу (методу сольве), а також в ході комплексної переробки нефелінів.
Гігроскопічний продукт, на повітрі поглинає вологу і вуглекислоту з утворенням кислої солі nahco 3 , при зберіганні на відкритому повітрі злежується. Водні розчини карбонату натрію мають сильно лужну реакцію. Випускають карбонат натрію технічний (натрій вуглекислий) марки а (гранульований) і марки б (порошкоподібний).
Сода-загальна назва технічних натрієвих солей вугільної кислоти. Карбонат натрію ( кальцинована сода, натрій вуглекислий) – хімічна сполука na 2 co 3 , натрієва сіль вугільної кислоти.
Карбонат натрію-сіль, утворена катіоном натрію і аніоном вугільної кислоти.
Кальцинованої содою називається безводний карбонат натрію na 2 co 3 . Кальцинованої вона називається тому, що отримують її прожарюванням (кальцинуванням) гідрокарбонату натрію nahco 3 або кристалогідрату карбонату натрію, наприклад, na 2 co 3 .10h 2 o.
Міжнародна назва: sodium carbonate.
Сода – загальна назва технічних натрієвих солей вугільної кислоти.
– na 2 co 3 (карбонат натрію) – кальцинована сода.
– na 2 co 3 .10h 2 o (декагідрат карбонату натрію, містить 62,5% кристалізаційної води) – кристалічна сода; іноді випускається у вигляді na 2 co 3 .h 2 o або na 2 co 3 .7h 2 o.
– nahco 3 (гідрокарбонат натрію) – питна або харчова сода, натрій двовуглекислий, бікарбонат натріяназваніе «сода» походить від рослини salsola soda, з золи якого її добували, кальцинованої соду називали тому, що для отримання її з кристалогідрату доводилося його кальцинувати (тобто нагрівати до високої температури).
Сода була відома з давніх часів. Ще стародавні єгиптяни застосовували природну с. (з озерних вод) як миючий засіб, а також для варіння скла. До 18 ст.карбонати натрію і калію називали «алкалі», тобто лугом. У 1736 французький вчений а.л. Дюамель дю монсо вперше розрізнив ці дві речовини: перше стали називати содою (по рослині salsola soda, з золи якого її добували), а друге – поташем.
Знаходження в природі.

Кальцинована сода зустрічається в природі у великих кількостях, головним чином в соляних пластах у вигляді підземних грунтових розсолів, ропи в соляних озерах і мінералів. Також карбонат натрію зустрічається в золі деяких морських водоростей, а також у вигляді наступних мінералів:
– нахколит nahco 3 ;
– трону na 2 co 3 .nahco 3 .2h 2 o;
– натрон (сода) na 2 co 3 .10h 2 o;
– термонатрит na 2 co 3 .h 2 o.
На землі відомі понад 60 таких родовищ.
Сучасні содові озера відомі в забайкаллі і в західному сибіру; великою популярністю користується озеро натрон в танзанії і озеро серлс в каліфорнії. Трону, що має промислове значення, відкрито в 1938 у складі еоценової товщі грін-рівер (вайомінг, сша). Разом з троною в цій осадової товщі виявлено багато раніше вважалися рідкісними мінералів , в тому числі давсоніт, який розглядається як сировина для отримання соди і глинозему. У сша природна сода задовольняє понад 40% потреби країни в цьому корисному копалині. У нашій країні через відсутність великих родовищ карбонат натрію з мінералів не видобувається.
Історичні відомості про отримання соди.
Сода була відома людині приблизно за півтори-дві тисячі років до нашої ери, а може бути і раніше. Її добували з содових озер і витягували з нечисленних родовищ у вигляді мінералів натрону na 2 co 3 .10h 2 o, термонатрита na 2 co 3 .h 2 o і трони na 2 co 3 .nahco 3 .2h 2 o.
Перші відомості про отримання соди шляхом упарювання води содових озер відносяться до 64 року і наведені в творі римського лікаря діоскоріда педанія про лікарські речовини. І йому, і алхімікам всіх країн аж до 18 в .сода представлялася якоюсь речовиною, яке шипіло з виділенням якогось газу при дії на нього відомих на той час кислот-оцтової ch 3 cooh і сірчаної h 2 so 4.
Тепер відомо, що шипіння – це результат виділення газоподібного діоксиду вуглецю (вуглекислого газу) co 2 в результаті реакцій: na 2 co 3 + 2ch 3 cooh = na(ch 3 coo) + co 2 + h 2 о і na 2 co 3 + 2h 2 so 4 = 2nahso 4 + co 2 + h 2 о, де утворюються ще ацетат натрію na(ch 3 coo) і гідросульфат натрію nahso 4 .
За часів діоскориду педанія про склад соди ніхто не мав поняття, адже і діоксид вуглецю відкрив голландський хімік ян ван гельмонт (який назвав його «лісовим газом») тільки через шістсот років.
Штучну соду навчилися отримувати після довгих і болісних пошуків тільки в 18 ст.але спочатку слід було визначити склад цієї речовини, виділивши його в досить чистому вигляді. У 1736 французький хімік, лікар і ботанік анрі луї дюамель де монсо, користуючись водою содових озер і застосувавши метод перекристалізації, вперше виділив чисту соду. Йому вдалося встановити, що сода містить хімічний елемент «натр». Роком пізніше дюамель і німецький хімік андреас сигізмунд маргграф прийшли до висновку, що сода na 2 co 3 і поташ (карбонат калію k 2 co 3) – різні речовини, а не одне і те ж, як вважалося раніше.
Дюамель намагався отримати соду, діючи оцтовою кислотою ch 3 cooh на сульфат натрію na 2 so 4 . З точки зору сучасного хіміка, це абсолютно безглуздо, але дюамель не знав складу ні того, ні іншого з узятих ним вихідних речовин. Йому було також невідомо, що сильну кислоту (сірчану) не можна витіснити з солей слабкою кислотою (оцтової). Проте, дюамель зробив цікаве спостереження: при нагріванні суміші сульфату натрію з оцтовою кислотою почали виділятися пари, які загорілися від полум’я свічки. Це була досить летюча і горюча оцтова кислота.
Історія знає чимало інших, іноді і небезпечних спроб отримати соду. Так, маргграф з цією метою змішував нітрат натрію з вугіллям, а потім нагрівав суміш. Досвід завершився спалахом суміші, яка обпекла йому обличчя і руки. Маргграф не врахував, що достатньо до суміші нітрату натрію (натрієвої селітри) і вугілля додати сірку, як вийде один з видів пороху.
Правда, при проведенні реакції 4nano 3 + 5c = 2na 2 co 3 + 3co 2 + 2n 2 вдалося отримати трохи соди, але якою ціною!
Перший промисловий спосіб отримання соди зародився в росії. У 1764 російський хімік, швед за походженням академік ерік густав лаксман повідомив, що соду можна отримати спікання природного сульфату натрію з деревним вугіллям. При цьому протікає реакція: 2na 2 so 4 + 3c + 2o 2 = 2na 2 co 3 + co 2 + 2so 2 . Тут крім карбонату натрію na 2 co 3 утворюються два газоподібних речовини – діоксид вуглецю co 2 і діоксид сірки so 2 .

Лаксман здійснив отримання соди за своїм способом в 1784 на власному скляному заводі в тальцинську недалеко від іркутська. На жаль, подальшого розвитку цей спосіб не отримав і незабаром був забутий. Але ж ще петро i в 1720, відповідаючи на питання князя голіцина, навіщо потрібна «зода», писав: «зодою пом’якшують шерсть». У 1780 російський академік гільденштедт зазначав, що «свербіння можна почесть важливим товаром в російській торгівлі. Склярі і фарбувальники багато її витратять, а надалі ще й більше оной розходитися буде, коли більше стануть робити білих стекол».
«зодою» або “сверблячкою” називали в росії соду. Незважаючи на велику кількість власної сировини для виробництва соди її ввозили в росію з-за кордону аж до 1860.
У 1791 французький лікар і хімік-технолог нікола леблан, нічого не знаючи про спосіб лаксмана, отримав патент на «спосіб перетворення глауберовой солі в соду» (глауберова сіль – декагідрат сульфату натрію na 2 so 4 .10h 2 o). Леблан запропонував для отримання соди сплавляти суміш сульфату натрію, крейди (карбонату кальцію) і деревного вугілля. В описі винаходу він вказував: “над поверхнею плавиться маси спалахує безліч вогників, схожих на вогні свічок. Отримання соди завершується, коли ці вогники зникають”.
При сплавленні суміші протікає відновлення сульфату натрію вугіллям: na 2 so 4 + 4c = na 2 s + 4co. Утворився сульфід натрію na 2 s взаємодіє з карбонатом кальцію caco 3: na 2 s + caco 3 = na 2 co 3 + cas. Після повного вигорання вугілля і монооксиду вуглецю co (“вогникиПотенційних і вже відбулися клієнтів. А відповідно буде впливати і на рівень вашого доходу.
Зміст
Обладнання
У наш час пошук обладнання не складе труднощів. Проте, цей етап також вкрай важливий для забезпечення якісної роботи майбутнього кабінету томографії. Сучасний ринок медичних апаратів мрт і кт дозволяє вибирати з досить широкого спектру постачальників, яких можна розділити на групи.
- фірми, які за рахунок дешевої робочої сили здатні поставляти обладнання за порівняно невисоку ціну.
- компанії працюють з поставками обладнання вже колишнього у використанні.
- фірми, які займаються різними модифікаціями систем, відновлених компаніями виробниками.
Саме останній варіант-найбільш поширений серед підприємців-початківців у цій сфері. Пояснення цьому просте. Подібне обладнання за ціною в кілька разів виграє у інших постачальників і в той же час не сильно поступається за якістю новим зразкам. Однак на якому б варіанті ви не зупинилися, вибір повинен супроводжуватися оцінкою фахівців в цій галузі. Так як, нагадаємо, від тих систем, які ви будете використовувати для діагностики пацієнтів залежить безпосереднє якість вашої роботи і обличчя фірми в цілому.
Додаткове оснащення
Крім власне апаратів кт і мрт, які є основою будь-якого кабінету томографії у вашій фірмі повинні бути присутніми і інші необхідні системи:
– сучасні комп’ютери, оснащені всім необхідним програмним забезпеченням для виведення результатів аналізів з апаратів кт і мрт.
– комп’ютери для безпосередньої адміністративної та бухгалтерської звітності
– витратні матеріали для апаратів томографії
– матеріали, що забезпечують своєчасний і належний догляд за обладнанням
– офісні меблі
– інше (сюди можуть входити як засоби для забезпечення комфортного очікування клієнтів, так і необхідні засоби для підтримки чистоти).
Витрати, доходи і термін окупності
Витратна частина розраховується при плануванні бізнесу завжди індивідуально, так як складається з безлічі факторів. Наприклад, оренда приміщення буде варіюватися виходячи з того в якому регіоні, місті, і навіть районі міста ви плануєте відкрити кабінет томографії. А вартість обладнання на ринку навіть одного і того ж типу може змінюватися в залежності від економічної ситуації в країні, курсу валют і рівня попиту. Однак спробуємо привести усереднені варіанти цін і рівня витрат на відкриття.
– оренда приміщення – від 2 до 7 тисяч доларів.
– апарат мрт – до 800 тисяч доларів.
– апарат кт – до 120 тисяч доларів.
– зарплатний фонд співробітників – від 7 до 15 тисяч доларів.
– оформлення документації, а також ліцензування діяльності – від 3 до 7 тисяч доларів.
– меблі та оргтехніка – до 7 тисяч доларів.
– спеціалізоване програмне забезпечення – від 10 до 30 тисяч доларів.
– витратні матеріали – від 10 до 40 тисяч доларів.
– інші витрати – до 20 тисяч доларів.
Підсумок-на страту може піти від півмільйона до мільйона доларів.
Через дорожнечу самого обладнання термін окупності подібного бізнесу сильно зростає. І при грамотному підході може становити від 2-х до 4-х років.
Однак навіть незважаючи на такий високий цінник старту і чималий термін окупності, приватний кабінет томографії визнаний вигідним і прибутковим бізнесом. І якщо ви зумієте подолати стартовий поріг вкладень, влаштувавши якісний набір послуг і постійно поповнюється базу клієнтів, то отримаєте не тільки бізнес, що приносить користь людям, але і вкрай прибуткова справа, що дозволяє отримувати після виходу на чистий прибуток дуже і дуже непоганий заробіток.
На рік.
Спосіб леблана.
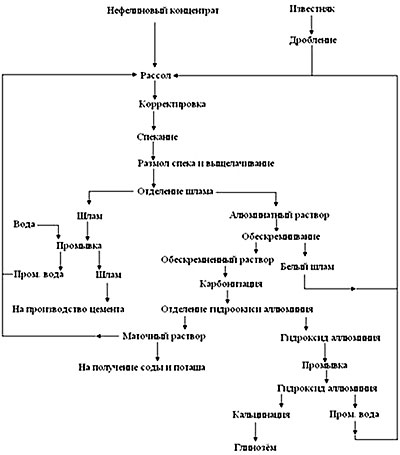
У 1791 році нікола леблана отримав патент на «спосіб перетворення глауберової солі в соду». У 1791 у франції було розпочато виробництво с.за його методом. Він складався з наступних стадій. Кам’яну сіль nacl дією концентрованої h 2 so 4 перетворювали в сульфат натрію: 2naci + h 2 so 4 = na 2 so 4 + 2hcl.
При температурі близько 1000° c запікається суміш сульфату натрію (»глауберової солі”), крейди або вапняку (карбонату кальцію) і деревного вугілля. Вугілля відновлює сульфат кальцію до сульфіду: na 2 so 4 + 2c → na 2 s + co 2 . Сульфід натрію реагує з карбонатом кальцію: na 2 s + сасо 3 → na 2 co 3 + cas.
Отриманий розплав обробляють водою, при цьому карбонат натрію переходить в розчин, сульфід кальцію фільтрують, потім розчин карбонату натрію упарюють. Сиру соду очищають перекристалізацією. Процес леблана дає соду у вигляді кристалогідрату na 2 co 3 .10h 2 o, що містить близько 62,5% води. Тому отриману соду доводилося для зневоднення нагрівати до червоного, кальцинувати, звідси кальцинована сода.
Сульфат натрію отримували обробкою кам’яної солі (хлориду натрію) сірчаною кислотою: 2nacl + h 2 so 4 → na 2 so 4 + 2hcl. Побічними продуктами були hcl (його спершу випускали на повітря, а потім стали поглинати водою, отримуючи технічну соляну кислоту) і cas (який утворював величезні відвали).
Перший в росії завод, який виробляв карбонат натрію таким способом, був заснований промисловцем м. Прангом в барнаулі в 1864 році.
Після появи більш економічного (не залишається у великих кількостях побічний сульфід кальцію) і технологічного способу сольве, заводи, що працюють за способом леблана стали закриватися. До 1900 90% підприємств виробляли карбонат натрію за методом сольве, а останні фабрики, що працюють за методом леблана закрилися на початку 1920-х.в даний час весь штучно виробляється карбонат натрію виробляється за методом сольве.
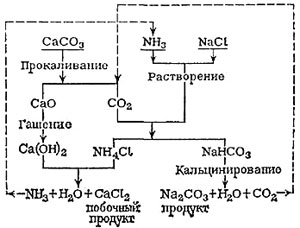
Спосіб хоу.
Розроблений китайським хіміком хоу (hou debang) в 1930-х роках. Відрізняється від процесу леблана тим, що не використовує карбонат кальцію.
За способом хоу в розчин хлориду натрію при температурі 40 градусів подається діоксид вуглецю і аміак. Менш розчинний гідрокарбонат натрію в ході реакції випадає в осад (як і в методі сольве). Потім розчин охолоджують до 10 градусів. При цьому випадає в осад хлорид амонію, а розчин використовують повторно для виробництва наступних порцій соди.
В даний час в ряді країн практично весь штучно виробляється карбонат натрію виробляється за методом сольве.
Електролізний процес.
Карбонат натрію можна також отримати за допомогою електролізного процесу. Водяна пара і діоксид вуглецю запускаються в катодне відділення установки з камерою діафрагмового типу для електролізу розчинів солей, де, взаємодіючи з їдким натром, вони перетворюють його в карбонат натрію.
Нефеліновий спосіб отримання кальцинованої соди.
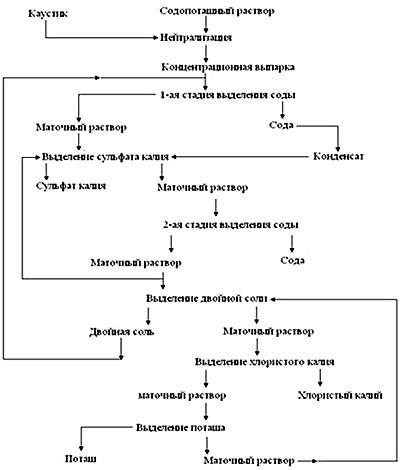
Для переробки нефелінової сировини в залежності від його складу і властивостей можуть бути застосовані різні способи. На малюнку показана технологічна схема комплексної переробки нефелінового концентрату способом спікання. Цей спосіб включає: 1) виробництво глинозему з отриманням в якості побічних продуктів содопоташного розчину і нефелінового шламу; 2) виробництво соди і поташу з содопоташного розчину; 3) виробництво цементу з нефелінового шламу.
З розробкою і впровадженням способу спікання в промисловість вперше була вирішена проблема комплексної переробки нефелінових концентратів, одержуваних при збагаченні апатитонефелінових порід кольського півострова. Однак значення способу спікання не обмежується переробкою кольських нефелінових концентратів. У нашій країні цей спосіб успішно застосовується також для переробки кияалтирських уртитів без попереднього збагачення, а також може бути застосований для переробки інших видів нефелінової сировини.
Переробка содопоташних розчинів.

Основними компонентами содопоташного розчину є na 2 co 3 , k 2 co 3 , k 2 so 4 і ксl. Розчин, отриманий методом двостадійної бікарбонатної карбонізації, містить також n-3 .
Для отримання соди і поташу розчин упарюють; різна розчинність соди і поташу дозволяє здійснити їх роздільне отримання. Розчинність поташу, у воді з підвищенням температури безперервно збільшується і при 100° c становить 0,9%; розчинність соди збільшується з підвищенням температури до 32,5° c, а потім знижується і при 100° c становить 31,1%.
Нижче розглянута технологічна схема переробки содопоташного розчину, одержуваного при комплексній переробці кіяшалтирських уртитів. Приблизний склад цього розчину, г / л: na 2 co 3 130; k 2 со 3 22; k 2 so 4 10; ксl 1,2.
Технологічний процес переробки содопоташного розчину складається з наступних основних стадій: нейтралізації вихідного розчину, концентраційної випарювання розчину і розчинення в ньому подвійної солі, першої стадії виділення соди, виділення сульфату калію, другої стадії виділення соди, виділення подвійної солі, виділення хлориду калію, виділення поташу.
Вміщені в розчині бікарбонати натрію і калію нейтралізуються в гідросмішувачі розчином каустичного лугу: nahco 3 +naoн=na 2 co 3 +h 2 o. Нейтралізація необхідна для попередження корозії апаратури, а також для того, щоб не допустити виділення в осад міститься в розчині гідроксиду алюмінію. Вміст каустичного лугу і нейтралізованому розчині, і перерахунку на na 2 о становить 0,1 – 0,15 г/л.
В результаті концентраційної випарки отримують розчин, з якого не кристалізуються солі (щільність упареного розчину 1,28-1,30 г/см3), що дозволяє видалити з такого розчину значну частину води на високопродуктивних багатокорпусних випарних батареях. Концентрований розчин після розчинення в ньому подвійної солі упарюють до концентрації, при якій відбувається кристалізація соди (щільність рідкої (рази 1,38-1,42 г/см3).
У продукційному корпусі батареї підтримують температуру 93-96° c, при якій в тверду фазу виділяється одноводна сода na 2 co 3 .h 2 o (сода-1). Якщо температуру в продукційному корпусі підняти до температури кипіння розчину при атмосферному тиску (106-108° c), то в тверду фазу буде виділятися безводна сода. Однак ця температура дуже близька до температури переходу безводної соди в одноводну. Неминучий перехід частини безводної соди в na 2 co 3 .h 2 o супроводжується цементацією осаду, що ускладнює відділення твердої фази від рідкої.
Тому отримання безводної соди на даній стадії випарювання недоцільно, сода-1 характеризується невеликим вмістом домішок поташу і сульфату калію; її відокремлюють від маточного розчину і направляють на сушку.
Сульфат калію k 2 so 4 виділяється при охолодженні до 35-40° c маточного розчину моногідратної соди, до якого для збільшення вмісту калійних солей додають частину маточного розчину безводної соди. Крім того, перед кристалізацією сульфату калію в розчин додають конденсат, щоб загальна лужність розведеного розчину в перерахунку на соду була в межах 420-450 г/л .у таких умовах відбувається кристалізація сульфату калію з відносно невеликим вмістом домішок соди, поташу і глазериту 3 k 2 so 4 .na 2 so 4.
Після виділення сульфату калію матковий розчин упарюють і виділяють з нього соду-2. Температура кипіння розчину в продукційному корпусі 108-115° c, тиск близько до атмосферного, щільність рідкої фази суспензії 1,45-1,5 г/см3. У цих умовах відбувається кристалізація безводної соди. Високий вміст поташу в розчині знижує температуру переходу безводної соди в моногідратну до 70-80° c, тому цементуючого осаду не утворюється. У порівнянні з содою – 1 сода-2 значно більше забруднена домішками поташу і сульфату калію.
У маточному розчині безводної соди ще залишається 10-12% na 2 co 3 , і при упаривании цього розчину в тверду фазу виділяється не поташ, а подвійна сіль (na,к) 2 со 3 . Кристалізацією подвійної солі досягається очищення розчину від соди. Для цього матковий розчин безводної соди змішують з маточним розчином поташу і отриманий розчин упарюють до досягнення щільності рідкої фази 1,64-1,66. Подвійну сіль повертають на першу стадію виділення соди. Матковий розчин подвійної солі розбавляють конденсатом до загальної лужності 520-550 г/см3 в перерахунку на соду і охолоджують до 10-30° c. При охолодженні з розчину виділяється в тверду фазу хлорид калію ксl, що необхідно для отримання поташу високої якості. Чим нижче температура кристалізації, тим повніше виділяється хлорид калію з розчину.
Очищений від хлору розчин упарюють при атмосферному тиску доЩільності рідкої фази 1,64-1,7 г/см3, після чого охолоджують до 55-75° c. При охолодженні, з розчину кристалізується півтораводний поташ до 2 со 3 -1,5 h 2 o. Що залишився після кристалізації поташу матковий розчин повертають на випарку з виділенням подвійної солі. Частина поташного маточника, але міру накопичення в ньому каустичної лугу і з’єднань алюмінію направляють в глиноземне виробництво.
Концентруюча випарка здійснюється в багатокорпусних прямоточних батареях, що складаються з випарних апаратів плівкового випаровування. Розчини з виділенням соди упарюють в 3-4 – корпусних випарних батареях, що працюють за прямоточною або змішаною схемою. Так як упарювання супроводжується значним виділенням твердої фази, то застосовують випарні апарати з примусовою циркуляцією, створюваної циркуляційним насосом. Упарювання розчинів з виділенням подвійної солі здійснюється в двокорпусних протиточних батареях. Висока концентрація солей в розчинах і відповідно висока їх депресія (30-35° c) не дозволяє застосовувати на цій стадії випарні батареї з більшою кратністю використання пари. При виділенні поташу розчин упарюють в однокорпусних випарних установках.
Для кристалізації сульфату калію, хлористого калію і поташу застосовуються двокорпусні вакуум-кристалізаційні установки, в яких охолодження розчину досягається за рахунок вакуумного випаровування частини води. Кожен корпус вакуум-кристалізаційної установки складається з вакуум-випарника і кристалорастителя. У вакуум-випарнику відбувається самоіспареніе розчину і його охолодження. Охолоджений розчин стікає в кристалораститель, де здійснюється зародження і зростання кристалів. Температура надходить у вакуум-випарник розчину перевищує температуру його після самоіспаренія всього лише на 2-5° c, тобто це означає, що ступінь пересичення розчину дуже невелика.
Це досягається змішанням в певному співвідношенні вихідного розчину з уже охолодженим розчином з кристалорастітеля. Змішаний розчин циркуляційним насосом полается в вакуум-випарник. Завдяки малому пересичення розчину кристалізується сіллю виходять досить великі кристали.відділення кристалів солей від рідкої фази здійснюється на центрифугах або безпосередньо, або з попереднім згущенням солей в згустителях.
Для сушіння солей застосовують барабанні і аерофонтанні сушарки. Аерофонтанная сушарка являє собою вертикальну трубу з декількома перетисками по висоті. Завдяки пережимам відбувається інтенсивне перемішування матеріалу з гарячими газами і збільшується час перебування його в сушарці. Гарячі топкові гази надходять в сушарку знизу і підхоплюють вологий матеріал, який подається в сушарку живильником. Температуру теплоносія (топкових газів) па вході в сушарку підтримують при сушінні (кальцинації) соди 700-800° c, при кальцинації поташу-близько 700° c. Висушений матеріал відділяється від газів в циклонах. Після очищення і пінних газоочисниках гази викидаються в атмосферу.кальцинована сода з нефелінового сировини повинна задовольняти вимогам гост 10689-75. Основні області застосування цієї соди: виробництво глинозему і нікелю, скляна і целюлозно-паперова промисловості.
Виділяються з содопоташних розчинів сульфат калію і хлористий калій використовують в сільському господарстві в якості калійних добрив.
Основні напрямки використання:
– харчова промисловість (використовується як регулятор кислотності);
– шкіряна промисловість;
– виробництво скла;
– целюлозно-паперова промисловість;
– виробництво мила;
– хімічна промисловість (виробництво синтетичних миючих засобів і лакофарбових матеріалів);
– чорна металургія (виробництво чавуну).
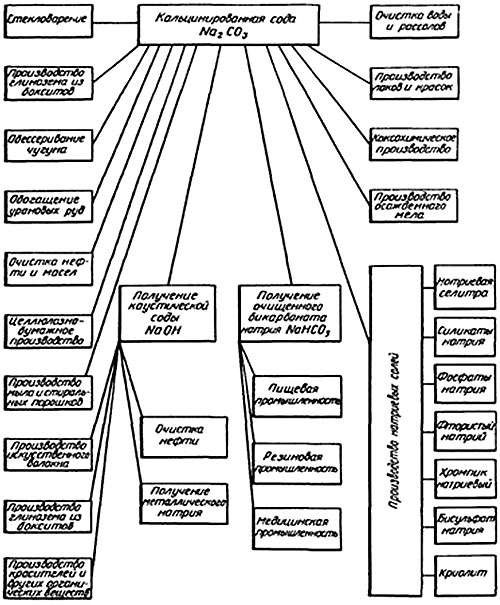
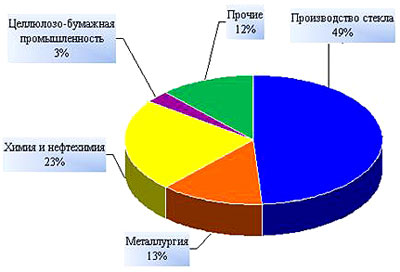
Застосування кальцинованої соди в різних секторах промисловості надзвичайно різноманітне. У найбільших кількостях вона застосовується в скляній промисловості. Крім того, карбонат натрію широко використовується в кольоровій металургії, хімічній і нафтохімічній, нафтопереробній промисловості, електронній, миловарній, жировій, харчовій, текстильній, целюлозно-паперовій галузі вітчизняної економіки, а також у виробництві товарів побутового призначення і поставки на експорт.кальцинована сода є одним з найважливіших продуктів хімічної промисловості. У найбільших кількостях продукт застосовується в якості компонента шихти при виробництві скла, при випуску мила та інших миючих засобів, емалей, для отримання ультрамарину, а також в процесах виробництва каустичної соди та інших натрієвих солей (наприклад, na 2 b 4 o 7). Карбонат натрію-вихідний продукт для отримання naoh, na 2 b 4 o 7 , na 2 hpo 4 .
Карбонат натрію знаходить широке застосування при знежиренні і рафінуванні металів, десульфуризації доменного чавуну і обробці бокситів у виробництві алюмінію, хімводоочищення, виробництві пластмас і синтетичних смол, при обробці золотоносних і уранових руд, для виробництва миючих засобів і в побуті. Використовується з’єднання і при варінні целюлози, дубленні шкіри і пом’якшенні води парових котлів і взагалі усунення жорсткості води, а також для нейтралізації кислих компонентів в промислових стоках і при очищенні нафтопродуктів, для отримання пігментів, напр. Fe 2 o 3 з fecl 3 . Зручний у використанні, карбонат натрію застосовується при обробці і знежиренні харчового обладнання.
У харчовій промисловості використовується в якості емульгатора (харчова добавка e500), регулятора кислотності, розпушувача, що перешкоджає грудкування і злежування.
Залежно від призначення технічна кальцинована сода повинна виготовлятися марок а і б.продукт марки а використовується для виробництва електровакуумного скла та інших цілей, марки б – в хімічній, скляній та інших галузях промисловості.
Сода кальцинована марок а і б використовується у виробництві скла всіх видів, в тому числі: кришталю, оптичного і медичного скла, склоблоків, піноскла, силікату натрію розчинного, керамічних плиток, компонента фрітт для глазурей; чорної і кольорової металургії: для виробництва свинцю, цинку, вольфраму, стронцію, хрому, для десульфуризації і дефосфації чавуну, в очищенні газів, що відходять, для нейтралізації середовищ.
Для виробництва електровакуумного скла використовується сода кальцинована марки а вищого сорту зі строго нормованим гранулометричним складом.
Сода кальцинована марки б застосовується в хімічній промисловості для виробництва синтетичних миючих засобів і жирних кислот, при очищенні розсолів, у виробництві фосфорних, хромових, барієвих, натрієвих солей як карбонатсодержащее сировину, у виробництві гліцеринів, алілового спирту; целюлозно-паперової, аніліно-барвистою і лакофарбової і нафтової промисловості.
Сода кальцинована використовується також як миючий засіб, добре видаляє жир, до всіх плюсів соди кальцинованої додається здатність пом’якшувати воду. Вона так само застосовується для пом’якшення води при пранні і кип’ятінні тканин, миття порцелянової, фаянсової, емальованого посуду та інших господарсько-побутових цілей. Входить в рецептуру пральних порошків. Широко рекламований засіб “калгон” – від накипу в пральних машинах-складається з триполійфосфату натрію і соди кальцинованої.
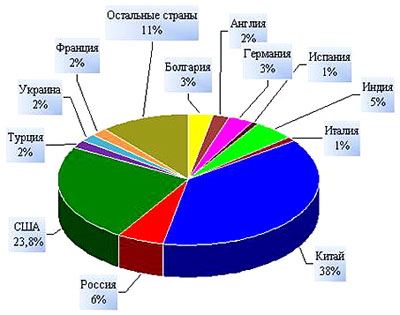
Дані споживання кальцинованої соди.
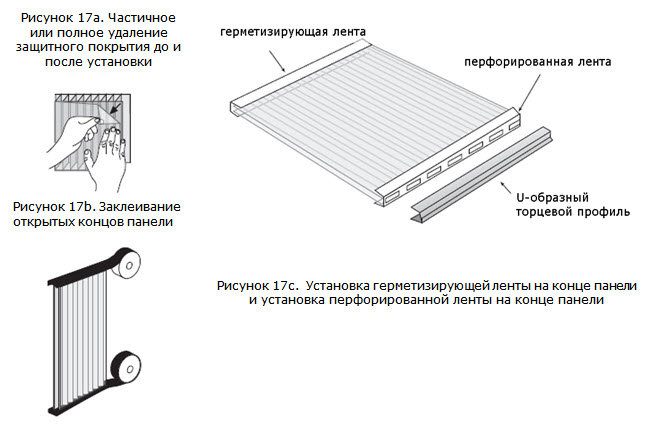
В якості інженерного пластика полікарбонат придбав велику популярність і популярність. Матеріал є лінійним поліефіром. У промисловості використовується тільки ароматична група даної речовини. На його основі створюються композиції, що відносяться до спеціальних полімерів. У промисловості технологія виробництва полікарбонату розділена на два основних етапи: синтез дрібнозернистого напівфабрикату і створення з нього листового будівельного матеріалу. Зазвичай їх здійснюють на різних підприємствах.
Виготовлення вихідної сировини
До недавнього часу промислове виготовлення гранул для подальшої переробки проводилося тільки методом міжфазної поліконденсації. Процес полімеризації при цьому відбувається на межі розділу рідини і газу, тобто двох фаз. Для виробництва використовуються двоатомний фенол і вугільна кислота (фосген). В реакції також беруть участь певний органічний розчинник і піридин, службовець і каталізатором, і акцептором.
До переваг даної методики, за якою іРозчиннику в присутності третинних органічних основ, що зв’язують соляну кислоту-побічний продукт реакції (спосіб поліконденсації в розчині);
Фосгенірованіе бісфенолів, розчинених у водному розчині лугу, на поверхні розділу фаз в присутності каталітичних кількостей третинних амінів (спосіб міжфазної поліконденсації);
Полікарбонат з’явився на будівельному ринку порівняно недавно, але вже встиг заслужити любов у архітекторів, будівельників, дачників. Його використовують для виготовлення навісів, теплиць, козирків.
Сьогодні на будівельному ринку представлена велика кількість компаній, що займаються виробництвом стільникового і монолітного полікарбонату. Найвідомішими і популярними марками є: ізраїльський полікарбонат polygal, європейський lexan, німецькі rodeca і makrolon, італійський policarb.
Однак, варто сказати і про російські марки полікарбонату. Це sellex, вироблений в місті чехів, казанський novattro і actual, московський carboglass, kronos з омська і novoglass з твері.
Про деякі вітчизняні марки полікарбонату ми і розповімо в цій статті.
Стільниковий полікарбонат sellex виготовляється на заводі «кронос», який є найбільшим виробником полікарбонату в росії.
За своїми характеристиками і якістю даний будматеріал ні скільки не поступається своїм європейським аналогами.
Стільниковий полікарбонат sellex виробляється на італійських технологічних лініях “omipa «з сировини найвищої якості німецької компанії»bayer”.
переваги полікарбонату sellex
Перевагою полікарбонату є чудова здатність розсіювати світло, а також висока світлопропускна здатність. Завдяки цьому даний матеріал широко використовується для влаштування парників, теплиць і навісів.
Матеріал володіє невеликою вагою і в той же час хорошою міцністю і підвищеною стійкістю до ударних навантажень. З полікарбонату sellex виготовляють рекламні короби і вивіски, і інтер’єрів, і для павільйонів і зупинок транспорту, склеюють дахи і віконні прорізи.
Стільниковий полікарбонат випускається в листах розміром 2,1 х 12 м., що дозволяє виготовляти з нього складні інженерні конструкції. Sellex представлений в декількох категоріях:» eko vice «і»sellex premium”.
Листовий полікарбонат sellex випускається в червоному, зеленому, прозорому, бірюзовому, молочному, синьому, жовтому і бронзовому кольорі. Основні випускаються товщини: 4,6,8,10,16 мм.
стільниковий полікарбонат novattro
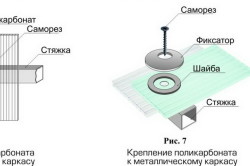
Листи novattro підходять будівництва надземних пішохідних переходів, зупиночних павільйонів, шумозахисних екранів, вітрин, енергозберігаючих фасадів і покрівлі складів, промислових теплиць, а також балконів, лоджій, терас, і багатьох інших конструкцій.
Продукція компанії safplast innovative буває трьох видів:
- novattro — лист без захисту від ультрафіолетового випромінювання для застосування всередині приміщення
- novattro uv1 — лист, що має з одного боку екструдовану захист від уф-випромінювання
- novattro uv2 — лист з двостороннім екструдованої захистом від уф-випромінювання.
Товщини листів стільникового полікарбонату novattro може бути 4,6,8,10,16,20,25,32 мм. Листи мають розмір 2,1 х 6 м. Або 2,1 х 12 м.
Листи полікарбонату товщиною 4,6,8 і 10 мм мають 13 стандартних кольорів, серед яких сірий колір, до складу якого входить спеціальна речовина, що надає металевий блиск поверхні.
Стільниковий полікарбонат novattro відповідає гост-30244-94.
стільниковий полікарбонат carboglass

Листи полікарбонату стільникового випускаються в 14 кольорах: бронза, коричневий, колотий лід, червоний, бордовий, жовтий, зелений, колотий лід коричневий, молочний, колотий лід бронза, прозорий, сріблястий, синій і бірюза.
До основних властивостей стільникового полікарбонату carboglass можна віднести надвисоку ударну міцність, захист від уф-випромінювання, за який відповідає спеціальний шар, нанесений на зовнішню поверхню листів, чудову світлопроникність (до 86%), відмінну стійкість до атмосферних впливів, міцність на розрив матеріалу і вигин.
Полікарбонат марки carboglass також знайшов застосування в будівництві стадіонів, спортзалів, басейнів, альтанок, душових кабін, пішохідних переходів, дверей, козирків, і оформленні вітрин.
Як бачите, виробництво стільникового полікарбонату не стоїть на місці, а розвивається семимильними кроками. Для споживача пропонується безліч варіантів кольору і товщини листів матеріалу. Вибір залишається лише за покупцем і цілей, які він переслідує.